저번 포스팅에 이어, IND 신청 절차에 대해 다뤄보겠습니다.
내 연구가 IND 승인 대상인지 알아보는 방법은 이전 포스팅 참고 부탁드립니다.
2021.06.07 - [분류 전체보기] - 연구자 주도 임상시험 IND 신청 방법 [1탄]
연구자 주도 임상시험 IND 신청 방법 [1탄]
연구자 주도 임상시험으로 IRB 신청 시, IND를 받아오세요.라는 답변을 받는 경우가 있습니다. 이 연구가 왜 IND를 신청해야 하지?? 라는 생각도 드실 텐데요. 이번 포스팅에서는 IND는 어떠한 연구
multi.tistory.com
IND 승인 신청은 "의약품 안전나라"에서 하게 됩니다.
https://nedrug.mfds.go.kr/index
의약품안전나라
의약품등검색, 의약품 사이버민원, 제품 및 제조사 정보, 의약품광고검색, 규격기준정보 등 수록
nedrug.mfds.go.kr
회원 가입 및 로그인
들어가셔서 회원가입이 되어있지 않은 경우, 회원가입부터 합니다.
약관 동의와 본인인증을 거치면,
정보 입력 페이지가 있는데요.
연구자 주도 임상시험을 하는 경우, 소속 회사면은 작성하지 않으셔도 됩니다.

IND 신청 후, 이에 대한 민원처리과정에서 발생하는 담당자의 의견을 받아야 하기 때문에, 정확한 e-mail 주소가 필요합니다.
마찬가지로, 민원 신청 정보에 대한 알림을 받는것도 카카오톡이나 문자로 받을 수 있습니다. 편하신 방법으로 신청하시기 바랍니다.
회원가입이 다 된 경우, 로그인 하시면 됩니다.
IND 신청
1. 상단의 전자민원/보고 tab을 누르시면
아래 사진처럼 나오는데요. 여기에서 전자민원 신청을 눌러주시면 됩니다.

2. 드롭다운 리스트에서 의약품 클릭하시고,

3. 임상시험계획승인을 작성한 후 검색하면,
민원 사무목록이 뜨는데요. 4번을 누르시면 됩니다.

4. 민원 사무 부류: 1차 분류명으로 연구자(학술연구용) 체크하시고, 2차 분류명으로 임상시험 체크하시고
그 후, 민원 신청하면 아래와 같은 화면이 뜹니다.

그러면, 이러한 페이지가 뜰 것입니다.

5. 하단으로 가시면 승인 또는 변경 시 체크리스트 양식을 다운받아 구비 서류에 첨부하라고 되어있는데요.
양식(임상시험계획 승인 제출자료 체크리스트) 다운로드 받으시면 됩니다.
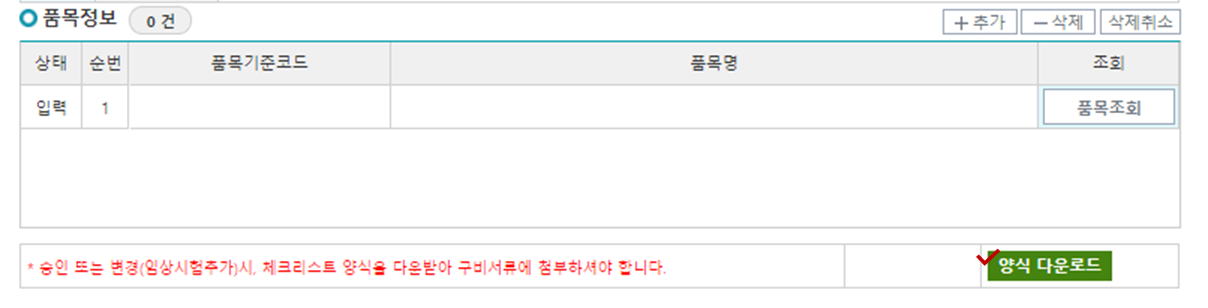

해당하는 번호로 가시면
예를 들어, 연구자 임상 3번으로 가시면
아래와 같이 어떤 자료를 제출해야하는지가 나옵니다.
1, 2, 3, 4번은 연구계획서 쓰시고 IRB 승인받기 위해 구비하는 서류와 겹칠 것으로 보이나
5번 이후부터는 익숙하지 않으실텐데요.
5번과 7번의 경우, 시판된 의약품을 제조하는 제약회사에 문의하시면 되지만,
7번의 경우 간혹 기밀문서로 제공하지 않는 경우도 있습니다.
이럴 경우, 제품의 인서트지로 갈음하는 경우도 있습니다.

여기를 채우셔서 자료 제출 시 같이 제출하셔야 합니다.
업로드 위치는
페이지 하단에 보시면 이렇게 보이실텐데요.

구비서류를 누르시면 아래와 같은 화면이 켜집니다.
cloud에 업로드 하는 방식으로 업로드하시면 됩니다.
아래와 같이 업로드 하시고 어느 파일에 업로드했다는 것을 업로드 위치에 쓰시면 됩니다.

이렇게 필요한 서류가 구축이 되었다면, 이제 이 페이지를 하나하나 작성해 보시면 됩니다.

각각 tab에서 어떠한 점을 작성하면 되는지에 대해서는 다음 포스팅에서 좀 더 자세하게 다뤄보도록 하겠습니다.
'임상연구' 카테고리의 다른 글
| 상대위험도와 교차비의 관계 (0) | 2021.08.03 |
|---|---|
| 상대위험도와 교차비 (0) | 2021.08.02 |
| 범주형과 연속형 자료 (3) | 2021.08.02 |
| 연구자 주도 임상시험 IND 신청 방법 [3탄] (0) | 2021.06.08 |
| 연구자 주도 임상시험 IND 신청 방법 [1탄] (8) | 2021.06.07 |




댓글